

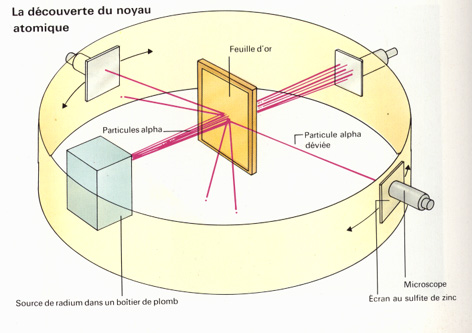
Le modèle atomique évolua lorsque Rutherford, Geiger et Marsden réalisèrent une expérience cruciale. Ils bombardèrent des feuilles d'or par des particules alpha (ce sont des particules de charge électrique positive double, issues de la radioactivité naturelle).
 |
 |
Ils constatèrent alors que ces "particules-projectiles" alpha étaient rarement déviées par les "atomes cibles" des feuilles d'or.
En effet, on observait généralement une légère diffusion due aux électrons.
Parfois, mais très rarement, on observait néanmoins une forte déviation d'une de ces particules alpha. Cela signifiait en fait que l'atome était formé d'une grande région diffuse peuplée de petits électrons et d'une petite partie centrale et concentrée de charge électrique positive (le noyau).
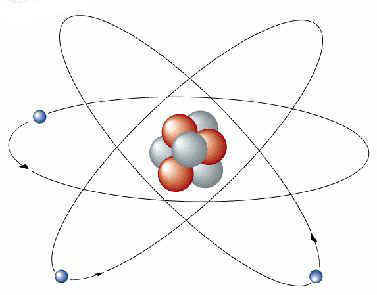
Finalement, les scientifiques se rendirent compte qu'il y avait d'immenses zones vides à l'intérieur des atomes. Ceci leur permit d'expliquer pourquoi la plupart des particules alpha n'étaient que peu déviées par l'influence électrique des charges atomiques (car elles sont trop éloignées).